PROFILAXIS DE LA CARIES
Elvira Agulló Lidón
El sellado preventivo-terapéutico es una medida protectora de la caries, incorporada en las nuevas prestaciones, que ofrece una protección ilimitada de las fosas y fisuras oclusales, si se realiza adecuadamente.
El diagnóstico radiológico de las lesiones proximales del esmalte ya es posible y se valora como alternativa al tratamiento con relleno. Si la zona radiotransparente llega hasta la unión amelodentinaria y el proceso carioso sobrepasa este límite, están indicadas las medidas restauradoras terapéuticas, que van desde la preparación de la cavidad hasta el tratamiento del canal radicular.
Los cambios en la preparación de cavidades son indiscutibles. De acuerdo con los principios básicos de la etiología de la caries y de las periodontopatías, y tratándose de personas con higiene bucal adecuada, ya no se realiza la extension for prevention ni la forma de caja. La nueva doctrina sobre rellenos exige un procedimiento conservador dirigido a la lesión, con delimitación de los bordes de la cavidad desde las zonas de autolimpieza hasta las de limpieza mecánica. La infraextensión o minipreparación de las cavidades proximales no se recomiendan, dado el estado actual de la higiene interdentaria.
Los sistemas de sellador-composite, los composites, las sustancias de retención de esmalte y dentina, los composites y los inlays de composite de alto poder, los cementos ionoméricos de vidrio y sus combinaciones con composites ofrecen nuevas perspectivas terapéuticas (Jordan,1989, 30). No obstante, aún no existe ningún relleno duradero de composite portador de oclusión para los dientes laterales. Sólo los especialistas pueden manipular las propiedades del composite que les hacen poco adecuado para el relleno desde el punto de vista técnico.
La placa está compuesta en un 60-80 % por microorganismos (García, 1997, 103). Las consideraciones generales son muy difíciles de exponer ya que la composición química y microbiana de la placa es muy variable y se modifica en función de la localización, el medio externo, la vida de la placa y la edad del individuo. La placa tiene una enorme importancia etiológica en la formación de la caries y en las periodontopatías.Además de estos factores (vida del sarro dentario, hábitos alimentarios, cuidado dentario, edad del individuo), la placa bacteriana posee un efecto cariógeno variable, ya que, dependiendo de su composición microbiana, los carbohidratos de la dieta se degradan a diferentes ácidos orgánicos (Subirŕ C; Cuenca E; Serra L, 1997, 49). Lo más importante es que la microflora local pueda tolerar los ácidos producidos, ya que estos también causan caries.
Depósito dentario
Se define como materia alba o blanca la acumulación de células epiteliales y microorganismos en la superficie dentaria sin una estructura determinada. Este tipo de sustancia no muestra crecimiento orgánico, ni posee actividad metabólica conocida y se elimina por cepillado. Los restos de comida también producen acumulaciones casuales primarias pero dependiendo de los lugares de retención. En cambio, la placa es un depósito de microorganismos y, por tanto, una cumulación local de consistencia blanda. La placa muestra una adherencia firme y estructurada, ya que la microflora penetra en el interior de su matriz. En función del medio externo, la microflora se diferencia y adquiere actividad metabólica específica. El depósito de calcio y fosfato de la saliva permite la formación de centros de cristalización, sobre los que se calcifica la placa con mayor o menos rapidez (Álvarez, 1999, 13). El cálculo dentario que se forma representa el estadio final del desarrollo de la placa y es metabólicamente inactivo. Sin embargo, no debe considerarse como un producto final inofensivo, ya que favorece la colonización por nuevas bacterias.
Los criterios de clasificación de los microorganismos de la flora de la placa bacteriana son simples, pero muy eficaces, ya se basan en una tinción de Gram y en la morfología microscópica de las bacterias. El grupo de cocos se diferencia con facilidad, mientras que el de bacilos y filamentos es extraordinariamente heterogéneo. Entre los representantes de los bacilos de pequeńo tamańo se encuentran los lactobacilos (gérmenes grampositivos) y Actinobacillus, Haemophilus y bacilos de tipo Bacteroides y Eikenella (bacterias gramnegativas). Corynebacterium, Eubacterium, Propionibacterium y los miembros de la familia Actinomycetaceae se diferencian de éstos por sus caracteres pleomórficos. Fusobacterium es un bacilo delgado y algo más largo, mientras que Capnocyitophaga es un filamento muy largo (fig.1).
|
| |||||
| aerobio, anaerobio facultativo | anaerobio | aerobio, anaerobio facultativo | anaerobio | ||
| cocos | Streptococcus S.milleri S.mitis S.mutans S.salivarius S.sanguis |
Peptostreptococcus | Neisseria | Veillonella | |
| bacilos y filamentos |
Corynebacterium Lactobacillus Familia Actinomycetaceae ACtinomyces Arachnia Bacterionema Rothia |
Eubacterium Propionibacterium |
Acinobacillus Capnocytophaga Eikenella Haemophilus |
Fusobacterium Leptotrichia Bacteroides Grupo B.-oralis B.gingivales |
|
| bacilos
espirilados | Campylobacter Tre p onema |
||||
Fig.1. Las especies más importantes de la microflora de la placa (Rateitschak y Wolf, 1984).
Las condiciones del medio de la placa en lo que respecta a la presión de oxígeno, efecto de la saliva, hábitos alimentarios y pH, dependen de la localización y de la placa y, por tanto, de su espesor (Subirŕ C; Cuenca E; Serra L, 1997, 500). Por este motivo, las placas de las fisuras y las placas subgingivales son estrictamente anaerobias, mientras que las placas supragingivales muestras una superficie aerobia y condiciones anaerobias en las capas más profundas. Estas condiciones ambientales influyen de forma decisiva en la composición microbiológica.
Metabolismo de la flora de la placa
El pH de la placa disminuye cuando los carbohidratos de los alimentos azucarados se difunden en ella, ya que es su degradación enzimática bacteriana determina la aparición de ácidos. Cuando la concentración de hidrogeniones oscilan entre valores de pH de 5,0-5,5 se alcanza una concentración crítica a partir de la cual se disuelve la apatita (Echevarría, 1995, 321). El tipo de carbohidratos y de microorganismos determina el tipo y cantidad de ácidos producidos, así como la rapidez de su formación. Cuando más vieja y espesa sea la placa, mayor es la posibilidad de que se reduzca el pH tras el consumo de soluciones de azúcar.
Los ácidos láctico, butírico, acético y propiónico son los más comunes, mientras que el fórmico y valeriánico son más raros.
Los estreptococos son los gérmenes que producen más ácido; estros microorganismos producen sobre todo ácido láctico a partir de la glucosa. Dependiendo de la concentración y distribución de las actividades enzimáticas del metabolismo intermediario, se diferencian la placa y el esmalte cariado o sano.
Muchos microorganismos sintetizan polisacáridos a partir de mono y disacáridos, y deben distinguirse los polisacáridos extracelulares (EPS) de los intracelulares(IPS). En cuanto a la patogenia de la caries, conviene recordar que los IPS pueden almacenarse y estar a disposición de los microorganismos como carbohidratos de reserva, que son degradados cuando falta el azúcar de la dieta. Los polisacáridos extracelulares se forman sobre todo a partir de la sacarosa, fructosa y glucosa. Los EPS, que constituyen un elemento activo de la placa, desempeńan un papel esencial en la patogenia de la caries y de la gingivitis. Aparte Streptococcus mutans , otras muchas bacterias que sintetizan EPS (Albers, 1988, 51). Esta matriz facilita la adherencia de los microorganismos a la superficie dentaria y su unión a otras bacterias de la microflora oral, que no son lavadas por la saliva. La producción de polisacáridos extracelulares es una actividad metabólica básica que permite la colonización microbiana de la superficie dentaria, pero no la única.
La adherencia de los microorganismos orales es la primera etapa del desarrollo de la placa. Así, la colonización microbiana, por microorganismos grampositivos, es paralela a la formación de la película dentaria o cutícula del esmalte. Estos microorganismos, además de formar EPS, tienen propiedades de absorción con ayuda de proteínas y enzimas especiales de la pared celular, y forman auténticos pseudópodos.
La localización predilecta de la placa inicial son los desgarros finos del esmalte, los márgenes de las encías y las imperfecciones. Más adelante, la acumulación de la placa se produce sobre todo en la superficie proximal y cervical, las localizaciones antes mencionadas y el sistema de fisuras y fosas.
Las relaciones interbacterianas entre los distintos tipos de gérmenes contribuyen a la capacidad de adhesión de los polisacáridos y a su fijación mecánica, con lo que se mantiene la integridad de la placa. Las fuerzas de unión entre los distintos tipos bacterianos pueden ser de gran especificidad.
Cálculo dentario
El cálculo dentario se reconoce en clínica como una modificación de la placa que alcanza en esta fase un volumen importante. La denominación cálculo dentario supragingival indica el depósito calcificado en sentido coronal a los márgenes de la encía. El cálculo dentario subgingival no es visible y se localiza bajo los márgenes de la encía en las bolsas gingivales y periodontales. Ambos tipos de cálculos se depositan sobre placas superficiales vitales, aún no mineralizadas, con una diferencia de dureza de 30kg/mm2 (Echevarría, 1995, 508-510). Por lo general, las placas y los cálculos supra y subgingivales se presentan de forma combinada. La placa se mineraliza con una velocidad variable, sobre todo en los conductos eferentes de las glándulas salivales mayores. Las localizaciones predilectas son la superficie lingual de los incisivos inferiores, superficie bucal de los molares superiores y superficie de la raíz del diente próxima a la bolsa (Fig.2). Los cálculos dentarios recientes o antiguos contienen cristales de fosfatos cálcicos.
El depósito alternante y periódico de capas mineralizadas de la placa con un trayecto paralelo a la superficie dentaria (que indica crecimiento por aposición), es una característica del cálculo dental antiguo.

Fig.2. Placa sobre fisura en la cara oclusal de un molar (Riethe, 1990, 5).
Se ha comprobado que casi todos los pueblos primitivos practicaban medidas intensivas de higiene bucal. “La limpieza dentaria es una necesidad generalizada, que los etnólogos indican expresamente lo contrario” (Albers, 1988, 102). Las medidas profilácticas se dirigen contra la placa microbiana. Estas medidas comprenden:
Reveladores-visualización de la placa
Los depósitos no calcificados son difíciles de localizar a simple vista. Este es el motivo de que se trate la placa con colorantes vitales o alimentarios (reveladores), con el fin de valorar el resultado de las medidas de higiene bucal tomadas por el odontólogo y el paciente. Entre los preparados más útiles se encuentran la solución de eritrosina y los comprimidos colorantes (Ávila, 1999, 82). La solución de eritrosina clásica se aplica con un palillo de algodón sobre la superficie dentaria y los márgenes de las encías(Fig.3). El odontólogo prefiere este tipo de solución, mientras que los pacientes suelen utilizar los comprimidos colorantes en su domicilio . La saliva se colores después de masticas estos comprimidos y se distribuye con la legua por la superficie dentaria y las encías durante 20seg, dejando que penetre adecuadamente en los espacios interdentales. A continuación se escupe el resto de saliva y se enjuaga la boca con agua dos veces.
Las zonas coloreadas de la superficie dentaria, espacios interdentales y encías se muestran al paciente en un espejo y se frotan con una sonda, iniciando de ese modo su educación y motivación para que use el cepillo dentario y los restantes métodos auxiliares.
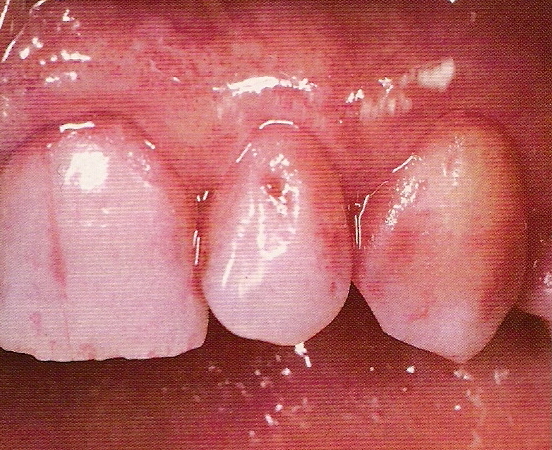
Fig.3. Indicador monocromático de placa. La eritrosina tińe de rojo la placa (Riethe, 1990, 16).
Cepillos dentales
Los cepillos dentales son un instrumente para la higiene bucal que permite la extracción mecánica de la placa y los residuos de alimentos de las superficies lisas de los dientes. Sin embargo, el espacio interdental y la profundidad de las fisuras no son tan accesibles. Los medios auxiliares para una higiene bucal y el sellado de fisuras completan este proceso de limpieza.
Los cepillos dentales deben adaptarse a las exigencias individuales de tamańo, forma y aspecto, y deben ser manejados con soltura y eficacia. Los cepillos no deben absorber humedad, se deben poder limpiar y conservar con facilidad y han de ser económicos. La fabricación de los cepillos se debe ajustar a los términos, medidas y requisitos de las normas DIN (Caries). Las investigaciones en este campo han determinado una serie de principios de fabricación que se aplican en los diferentes países, aunque estas normas no pueden considerarse definitivas. La utilidad de una adecuada limpieza con el cepillo para mantener la salid de los dientes y del periodonto se ha confirmado en múltiples estudios.
Los cepillos dentales se clasifican en blandos, intermedios o duros. Los blandos tienen el inconveniente de que no se consigue una fricción adecuada para extraer la placa (Wiegand; Attin, 2005,13-15). En la actualidad, se recomiendan cada vez más los cepillos blandos de cerda sintética para la conservación del tejido duro y de las partes blandas. Los cepillos ideales son aquellos de cabeza corta con una distancia pequeńa entre los distintos haces y puntas redondeadas.
La vida de los cepillos dentales es limitada. Se trata de artículos de consumo relativamente baratos en comparación con el tratamiento odontológico. Por otra parte, al ser un instrumento de uso diario, los cepillos sufren desgaste y la colonización microbiana se incrementa con el tiempo; por tanto, deben cambiarse cada 6 semanas, o a lo sumo cada 2 meses, y después de cualquier enfermedad oral o general. Existen algunos cepillos especiales como los cepillos para el espacio interdental, protésicos o de viaje, que complementan los tradicionales.
Higiene interdental
Hay diferentes métodos auxiliares, además del cepillo regular de los dientes y del uso de la pasta de dientes para la higiene interdental. Estos métodos se aplican para:
La seda dental se utiliza como medida de control en espacios interdentales estrechos y bajo los puentes, mientras que los palillos dentales se emplean para eliminar placas en espacios interdentales abiertos, surcos o restos impactados de alimentos (Wiegand; Attin, 2005,18). Cuando el espacio interdental es considerable, pueden utilizarse cepillos interdentales de distinto tamańo; otros métodos auxiliares, como los estimuladores, permiten llegar a lugares de difícil acceso, y también pueden utilizarse limpiapipas.
Pastas de dientes
Las pastas de dientes son sustancias cosméticas sin riesgo para la salud, siempre que se utilicen de acuerdo con las recomendaciones habituales. Se trata de preparados detergentes en forma de polvo, cristales o sustancia amorfa, junto con elementos líquidos que adoptan una consistencia de pasta en la relación de mezcla adecuada.
Su efecto limpiados radica en al eliminación de los depósitos bacterianos y no bacterianos (poder de limpieza), así como en un leve abrillantado de la superficie dentaria (poder de pulido), con un mínimo efecto abrasivo (poder de abrasión).
La sustancia limpiadora (sustancia abrasiva) reduce el tiempo necesario para extirpar los depósitos no calcificados. Las sustancias tensioactivas potencian el efecto de las sustancias limpiadoras por sus propiedades humidificadoras y su efecto de desprendimiento.
El principio activo de las pastas de dientes, por ejemplo el flúor, disminuye la incidencia de caries, aunque existe una gran controversia sobre el valor de los aditivos gingivotropos (Smyth; Taracida; Gestal, 1992, 23).
El uso de compuestos de flúor como principio activo de la pasta de dientes tiene como finalidad conservar los depósitos de flúor adquiridos en la fase pre y posteruptiva e intensificar su acumulación en el esmalte. Estas pastas tienen una concentración de flúor de 0,1- 0,15%, es decir, 1g de parta contiene 1,5mg de aditivo F, dosis inocua que, además, es diluida por los líquidos orales (transporte de flúor). Las pastas de dientes con flúor protegen contra la caries (siempre que no se inactive el principio activo) y ejercen un efecto profiláctico cuando se emplean diaria y continuadamente. La inhibición de la caries es aproximadamente del 25%, tanto en caso de consumo vigilado como no vigilado, si se exceptúan los “no colaboradores”. La utilización doméstica de pastas de dientes con flúor carece de riesgos para la salud. Por otra parte, se deben preparar pastas de sabor neutro para evitar el abuso de pastas infantiles con flúor aromatizadas como estimulantes del apetito.
Sellado de fisuras
Las fosas y fisuras, la colonización bacteriana y los sustratos impactados y retenido determinan de forma precoz una caries oclusal, debido a la falta de autolimpieza y a la reducción de la limpieza dentaria mecánica (Álvarez, 1999, 35). La superficie oclusal del diente apenas se beneficia de la aplicación de flúor, a diferencia de las caras lisas y proximales, aunque la aparición de lesiones cariosas en las zonas de fosas y fisuras puede evitarse mediante el sellado.
La eficacia clínica del sellado no depende tanto del grado de penetración del diacrilato en la profundidad de la fisura, después de realizar la técnica de corrosión del esmalte, como de la reacción entre la fisura y el ambiente microbiano, así como del bloqueo del aporte del sustrato hacia los microorganismos situados en la profundidad.
La caries de fisura es la lesión más frecuente entre nińos y adolescentes. Macroscópicamente, esta lesión se manifiesta como un cambio de color marrón oscuro o negro en las fosas y fisuras de los premolares y molares. La lesión adopta distintas coloraciones al microscopio óptico y puede extenderse o sobrepasar la unión amelodentinaria. Si no se realiza una intervención adecuada, la progresión es inevitable. Las condiciones locales favorecen la ausencia o disminución de limpieza espontánea.
Inicialmente, se demuestran microorganismos coloides grampositivos, que representan el 73-95% de los gérmenes vivos durante los 2 primeros días (Vega,1996, 20). El germen predominante es Streptococcus sanguis, mientras que Streptococcus mutans y los lactobacilos no son tan comunes en las placas recientes sobre fisuras, aunque su presencia se incrementa con el tiempo. Los bacilos y filamentos constituyen hasta un 12% de la población microbiana en las placas de 5 días de antigüedad.
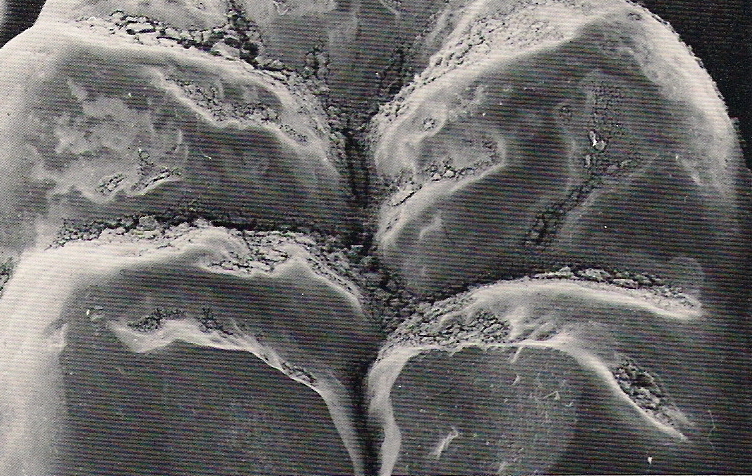
No se observan, en cambio, bacilos fusiformes, espirilares ni espiroquetas. La enorme variación de la microflora sugiere que cada fisura representa un sistema ecológico diferente. La disminución del número de microorganismos tras el sellado de las fosas y fisuras se ha confirmado en numerosos trabajos. Si las condiciones son adecuadas, las propiedades del sellador, óptimas y el sellado se efectúa con precisión, se obtiene una protección del 100% contra la caries, según todos los autores. Hasta el presente no se ha descrito la remineralización por el sellado (Fig.4).

Fig.4. Fisura. Fractura no tratada de un molar. Fisura extraordinariamente estrecha con forma de ampolla. FB=sueldo de la fisura. FW=pared de la fisura. S=esmalte. V=sellado (Riethe, 1990, 49)
Tejido dentario duro y su relación con el proceso cariógeno
El proceso carioso del esmalte, de la dentina y del cemento radicular es muy similar. En realidad, el esmalte puede descalcificarse simplemente por efecto de los ácidos. Sin embargo, para la disolución de la dentina y de cemento radicular se requiere la acción adicional de enzimas proteolíticas.El esmalte puede remineralizarse, tras la descalcificación cariosa inicial, por la presencia de iones protectores de hidroxifosfato cálcico y flúor en la cavidad bucal (Albers,1988, 17), pero la caries que sobrepasa la unión amelodentinaria determina cavitación y obliga a un tratamiento conservador.
La caries dentaria se extiende, dependiendo de la estructura, y penetra a lo largo del canalículo dentario, excavando la zona inferior al límite amelodentinario.
La caries radicular se observa en personas de edad avanzada, en la proximidad de la unión amelocementaria, y plantea serios problemas al odontólogo.
La caries dental es un proceso patológico localizado, de origen bacteriano, que determina la desmineralización del tejido duro del diente y finalmente su cavitación. La caries se inicia como una lesión microscópica, que alcanza finalmente las dimensiones de una cavidad macroscópica (Caries). Desde el punto de vista diagnóstico, hay que diferenciar entre:Etiología de la caries
De acuerdo con los conocimientos actuales, la formación, composición y metabolismo de la placa son esenciales para la aparición de reacciones en el periodonto marginal y la formación de lesiones cariosas (García,1997, 74).
Además de la significación etiológica de los microorganismos, existen otros componentes que deben reunirse para que aparezca la caries (Fig.5):
La caries se origina cuando la interrelación entre los microorganismos y su retención en la superficie dentaria (huésped) se mantiene un tiempo suficiente, ya que los productos metabólicos desmineralizantes (ácidos) alcanzar una concentración elevada en la placa por excesivo aporte de azúcares en la alimentación (sustrato).
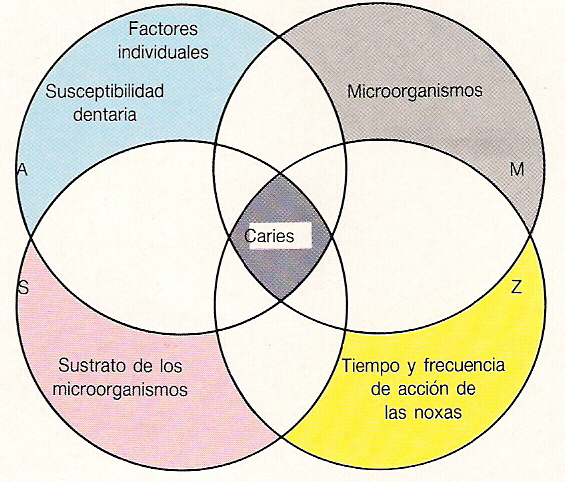
Fig.5. Etiología de la caries, condiciones indispensables. Esquema de la etiología multifactorial de la caries compuesto por 4 círculos que se solapan entre sí (Riethe, 1990, 70).
Caries incipiente
La lesión del esmalte aparece como una mancha opaca de aspecto brillante o mate, es reversible si se evitan los brotes frecuentes de descalcificación y las pausas neutrales relativamente prolongadas, la saliva se satura fácilmente de calcio y de fosfato y se aporta flúor de manera adecuada (Smyth; Taracida; Gestal,1992,93).
La lesión de “mancha blanca” se transforma en una mancha “marrón” como consecuencia de la absorción de sustancias exógenas. Hay que evitar una comprensión excesiva durante el sondaje para no producir cavitación.
Caries clínica
Este tipo de caries se caracteriza por la cavidad del esmalte, por lo que suele ser diagnosticada en la clínica y también tras el estudio radiológico. La desmineralización progresiva determina una transición de la descalcificación parcial del esmalte a la total, que se acompańa de pérdida de la continuidad de la superficie, invasión bacteriana, multiplicación de los microorganismos y penetración y excavación de la unión amelodentinaria. Por último, se produce la desmineralización y destrucción hística de la dentina.
Los microorganismos se dirigen desde la unión amelodentinaria hasta la pulpa a lo largo de los canalículos de dentina. La cuńa de caries dentaria se extiende de forma progresiva; cuando el proceso llega hasta la pulpa, se denomina caries profunda, término difícil de definir, que implica la pérdida de vitalidad de la pulpa si no se adoptan las oportunas medidas.
Pulpitis
La inflamación de la pulpa se produce por microorganismos, estímulos bioquímicos, mecánicos y térmicos, y sobre todo por caries de la dentina. Los síntomas clínicos rara vez se correlacionan con los hallazgos histopatológicos.
La reacción de la pulpa ante la infección producida por la caries se produce en un sistema cerrado.
La inflamación serosa y purulenta de la pulpa afecta una porción de la pulpa coronal (pulpitis parcial) o todo el tejido (pulpitis total).
Una vez que el proceso de la caries se abre a la cámara de la pulpa, los hallazgos histopatológicos y clínicos de ambas enfermedades son similares:
La pulpitis crónica clausa (inflamación cerrada) es la forma más frecuente de pulpitis crónica (Schäer; Rinn; Kopp, 1991, 64-66). La pulpitis crónica clausa se clasifica como una variante de los granulomas sistémicos.
La inflamación crónica de la pulpa suele originar necrosis hística: muerte celular y destrucción del tejido.
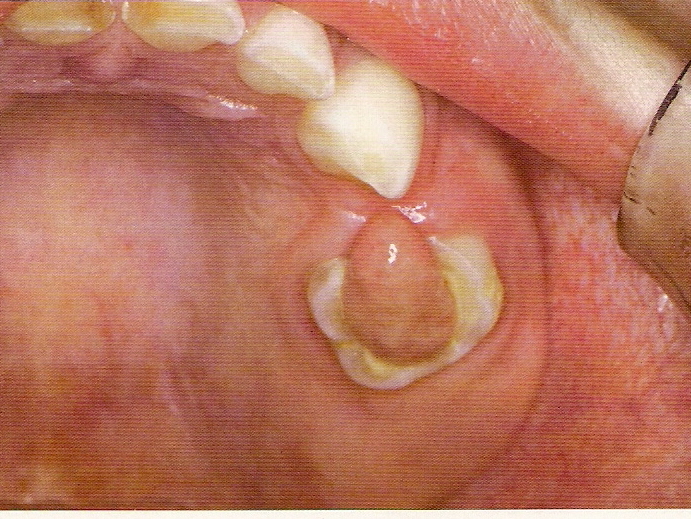
Fig.6. Pulpitis crónica abierta granulomatosa( poliploide). La figura muestra un pólipo pulpar epitelizado antiguo (Riethe, 1990, 84).
Conservación vital de la pulpa amenazada
El objetivo terapéutico consiste en conservar intacta la pulpa, manteniendo la cubierta dentinaria entre la cavitación y el espacio pulpar.
El método de recubrimiento indirecto consiste en dejar una capa delgada de dentina resistente a la sonda, aunque esté parcialmente infectada, entre la pulpa y el medio de recubrimiento (Ávila, 1999, 89). Este método consiste en mantener la vitalidad y estimulación de la producción de tejido duro por parte de la cubierta de dentina cerrada sometida al efecto medicamentoso.
El recubrimiento directo de la dentición permanente se basa en el adecuado cierre de la exposición pulpar en la dentina. El resultado depende del estado hístico de la pulpa tras la estimulación de la formación de dentina terciaria. Las condiciones para el recubrimiento directo son más favorables en las pulpas abiertas y puntiformes de los dientes juveniles. El recubrimiento directo, por otra parte, determina en ocasiones dolor o necrosis de la pulpa.
El recubrimiento directo de la dentición caduca resulta problemático, ya que plantea dificultades técnicas y sólo está indicado en caso de apertura accidental.
El método directo consiste en el tratamiento conservador de la pulpa abierta, de forma artificial o traumática con el fin de mantener su vitalidad.
La pulpotomía (amputación vital) consiste en extirpar el tejido coronal de la pulpa que aún conserva su vitalidad. La fase de defensa, curación y protección de la pulpa del conducto radicular recubierta con Ca(OH)2 es similar a la del recubrimiento directo.
El tratamiento de la pulpitis con preparados de corticoides y antibióticos se aplica para combatir rápidamente los dolores. Este tratamiento tiene como finalidad modificar por vía medicamentosa la pulpa expuesta y no expuesta.
Restauración con material plástico
El material de obturación para las cavidades proximales de los dientes incisivos consiste fundamentalmente en cemento de silicato. Sin embargo, la solubilidad e intolerancia de la pulpa a este material obliga a investigar nuevos sistemas químicos.
La base de partida de los nuevos materiales de obturación de cavidades son las resinas autotemplantes (polimerizados fríos). Las resinas PMMA (PPMA= metilmetacrilato polimerizado), aún no suficientemente estudiadas, han dado origen a diferentes materiales de obturación (Vega,1996, 53). Las resinas de obturación de los composites están formadas por compuestos orgánicos (matriz) y una sustancia de obturación inorgánica, unidos por silano. Estas resinas, basadas en el bis-GMA (bisfenol-A-glicidilmetacrilato) y en una molécula monomérica de gran tamańo desarrollada por Bowen, poseen unas características más adecuadas que el monómero de metilmetacrilato.
Alvarez H. 1999. Fundamentos, técnicas y clínica en rehabilitación bucal. Buenos Aires: Hacheace.
Ávila J. 1999. Última generación de materiales y técnicas aplicadas en odontología estética. Gaceta Dental, nş100: 84-96.
Caries. en: wikipedia (en línea). Disponible en http://es.wikipedia.org/wiki/Caries
Echevarría JM., Cuenca E. 1995. El manual de odontología. Barcelona: Masson.
García J. 1997. Patología y terapéutica dental. Madrid: Síntesis.
Jordan RE. 1989. Composites en odontología estética. Barcelona: Salvat.
Schäer R., Rinn LA., Kopp FR. 1991. Principios estéticos de la odontología restaurativa. Madrid: Doyma.
Smyth E., Taracida M., Gestal J. 1992. El flúor en la prevención de la caries dental. Madrid: Díaz de Santos.
Subirŕ C., Cuenca E., Serra L. 1997. Las pruebas salivales en el diagnóstico del riesgo de caries. Archivos de odonto estomatología, vol.13: 22-35
Vega JM. 1996. Materiales de odontología: Fundamentos. Madrid: Avances.
Wiegand A., Attin T. 2005. Influencia de las medidas de higiene oral en el desarrollo de defectos erosivos en la sustancia dental dura. Quintessence, vol.18:11-20
Bibliografía complementariaRiethe P. & al. 1990. Profilaxis de la caries y tratamiento conservador. Barcelona: Salvat.
Roig JL. 2008. Caries. Alzira: Bromera.
Bolsa gingival o periodontal: profundización patológica del surco gingival, una fisura patológica entre la parte interna de la encía y la superficie del diente.
Composite: material sintético que está compuesto por moléculas de elementos variados. Tales moléculas suelen formar estructuras muy resistentes y livianas.
Hiperemia: aumento en la irrigación a un órgano o tejido.
Inlay: técnica decorativa que consiste en insertar piezas de materiales coloreados en una depresión de un objeto base para moldear un diseńo o imagen.
Película dentaria o cutícula del esmalte: film suave, transparente, que precipita sobre las estructuras bucales, que permanece en aquellas donde no llegan los mecanismos de autolimpieza.
Pulpotomía: tratamiento realizado sobre dientes temporales en el que se elimina la pulpa correspondiente a la corona.