FACULTAD DE MEDICINA Y ODONTOLOGÍA
DEPARTAMENTO DE DERMATOLOGÍA
CUIDADOS ESPECIALES EN PROBLEMAS
DERMATOLÓGICOS
Dermatología Oncológica
Mónica Carulla Pascual
2º Odontología
Valencia, mayo 2006.
“No nos falta valor para emprender ciertas cosas que
son difíciles,
sino que son difíciles porque nos falta valor para
emprenderlas.”
1.- INTRODUCCIÓN:
a)
Epidemiología.
b)
Clasificación.
2.- TÉCNICAS DIAGNÓSTICAS BÁSICAS EN
DERMATOLOGÍA ONCOLÓGICA:
a)
Técnicas de biopsia cutánea.
b)
Métodos de biopsia:
I.-
Biopsia por rebanado o afeitado.
II.-
Biopsia en sacabocados (Punch).
III.-
Biopsia incisional.
IV.-
Biopsia escisional.
3.- CLASIFICACIÓN DE LAS NEOPLASIAS CUTÁNEAS:
3.1.- Carcinomas:
a)
Carcinoma basocelular.
b)
Carcinoma espinocelular.
3.2.- Neoplasias anexiales
cutáneas malignas:
a)
Carcinoma sebáceo.
b)
Carcinoma papilar.
c)
Carcinoma siringoide.
d)
Porocarcinoma.
e) Carcinoma anexial microquístico.
f)
Carcinoma adenoide quístico.
g)
Carcinoma mucinoso.
3.3.- Melanomas.
3.4.- Sarcoma de Kaposi.
3.5.- Otros angiosarcomas:
a)
Angiosarcoma NO ASOCIADO A LINFEDEMA
b) Angiosarcoma
Cutáneo asociado a Linfedema (Stewart-Treves)
c)
Angiosarcoma Radioinducido
d)
Otros:
●
Angiosarcoma epiteloide
●
Hemangioma endotelioma epiteloide
●
Hemangioma endotelioma retiforme
●
Angioendotelioma papilar endovascular (tumor de Dasbska).
4.- MELANOMAS:
4.1.-
Definición.
4.2.-
Epidemiología.
4.3.-
Factores de riesgo.
4.4.-
Factores pronósticos:
a)
Clínicos.
b)
Patológicos.
c)
Moleculares.
4.5.-
Clínica.
4.6.-
Tipos de melanomas:
a)
El melanoma de extensión superficial.
b)
El melanoma lentiginoso acral.
c)
El melanoma nodular.
d)
El lentigo melanoma maligno.
4.7.-
Métodos de diagnóstico.
4.8.-
Estadiaje.
4.9.-
Pronóstico.
5.1.-
Variedades clínicas:
a)
Clásica.
b)
Endémica.
c)
En relación con pacientes Transplantados.
d)
Epidémica asociada al VIH.
5.2.-
Histología.
5.3.-
Etiopatogenia.
5.4.-
Diagnóstico y diagnóstico diferencial.
5.5.-
Tratamiento.
5.6.-
Pronóstico.
6.- CONCLUSIÓN.
7.- GLOSARIO.
8.- PROCEDENCIA DE LAS IMÁGENES.
9.- BIBLIOGRAFÍA.
RESUMEN:
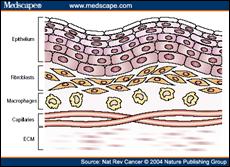
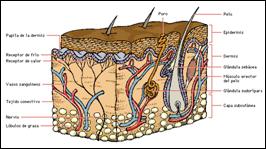
La piel es la capa más externa de nuestro
organismo, la que nos protege de las agresiones externas, la que delimita
nuestros órganos y tejidos, la que constituye una barrera hacia el exterior y
hacia el interior. En definitiva, nuestra “capa protectora”.
Pero todas estas funciones las tiene que
desarrollar ella sola, que al fin y al cabo es un tejido muy fino, débil y que
puede romperse fácilmente.
Entonces, ¿quién protege a la piel? La
respuesta es muy fácil, a parte de los propios mecanismos de defensa que tiene
la piel, nosotros somos los principales protagonistas de esa protección.
Seguro que a todos/as les gusta tener un
buen color de piel cuando llega el verano, y nos olvidamos de que hay ciertas
horas del día que son especialmente perjudiciales por las radiaciones UV que
llegan. En realidad, el hecho de que la piel se ponga morena, no es más que un
mecanismo de protección de la propia piel ante el “ataque” del sol.
A parte de este ejemplo, hay muchas más
situaciones en que tenemos que cuidar nuestra piel. Si no lo hacemos, pueden
producirse lesiones muy graves, algunas de ellas irreparables, aunque la
mayoría tienen solución.
Entre las graves, encontramos las
neoplasias benignas y malignas (cánceres), y de su estudio se encarga la
dermatología oncológica. Es importante conocer sus características, su
evolución y el tratamiento que tienen, ya que seguramente tendrán mejor
pronóstico de lo que podamos pensar.
Volver al índice
1.-
INTRODUCCIÓN:
El
cáncer de piel, en especial el melanoma, se beneficia de forma muy evidente de
campañas de prevención y, sobre todo, de detección precoz. Por esta razón,
desde hace algunos años se está haciendo bastante hincapié en el conocimiento
de la epidemiología y la fisiopatología de las neoplasias cutáneas. Además, se
realizan de forma constante avances en el diagnóstico y tratamiento de estas
patologías.
Por
otra parte, el cáncer cutáneo tiene un importante impacto emocional sobre los
pacientes. Éstos reciben con temor y angustia todo aquello cuya denominación
incluya términos tales como "-carcinoma" o, por supuesto,
"cáncer".
A) EPIDEMIOLOGÍA:
El cáncer de piel es el tipo más frecuente
de todos los cánceres. Se estima que alrededor del 50% de las personas mayores
de 65 años desarrollarán un cáncer de piel y que el 25% de ellos padecerán más
de uno a lo largo de su vida.
En todo
proceso neoplásico existen una serie de eventos consecutivos que se inician con
la aparición de una célula de crecimiento descontrolado y que culminan con el
desarrollo de diferentes clones celulares capaces de invadir, circular por la
sangre o linfa y sobrevivir y crecer en tejidos a distancia. Para que este
proceso tenga lugar deben coincidir una serie de factores predisponentes
individuales y/o ambientales. En el caso de los cánceres cutáneos, en general,
existen dos factores fundamentales que determinan la incidencia y prevalencia
de los mismos en las diferentes poblaciones: la radiación solar y el fenotipo
cutáneo.
- La radiación solar, en especial la
radiación ultravioleta, juega un papel fundamental en la etiopatogenia de la
carcinogénesis cutánea. Su importancia es diferente según el tipo de neoplasia
considerada.
En la radiación solar el tiempo
representa un factor añadido. Esto determina que la mayor parte de los
carcinomas acontezcan en pacientes de edad avanzada.
- El fenotipo cutáneo está definido
principalmente por el tipo de reacción de la piel ante la radiación solar. Esta
reacción determina que se tenga una mayor o menor sensibilidad a los efectos
nocivos de los rayos ultravioleta sobre el ADN nuclear.
Si se tiene en consideración estos dos
factores principales, se puede entender fácilmente que los países que tienen
una población predominante de piel clara y un clima soleado presentan las
mayores cifras de incidencia y prevalencia de cáncer cutáneo.
B) CLASIFICACIÓN:
Para la clasificación
de los tumores cutáneos malignos se ha considerado la célula o estructura a
partir de la cual se han desarrollado:
|
Célula originaria |
TUMOR |
|
Queratinocito |
Carcinoma
basocelular y espinocelular |
|
Anejos cutáneos |
Tumor anexial |
|
Melanocito |
Melanoma |
|
Vasos |
Sarcoma de Kaposi y
otros angiosarcomas |
Fig. 1: Relación de tumores con su célula originaria.
A
continuación describiré las técnicas que se utilizan para el diagnóstico de
cánceres en la piel y haré una clasificación para ver todas las variedades de
neoplasias cutáneas que se han descrito hasta el momento. Además detallaré dos de
estas neoplasias: el melanoma, que es el más frecuente, y el Sarcoma de Kaposi,
que aunque no muy frecuente, es una variedad muy peculiar.
Volver al índice
2.-
TÉCNICAS DIAGNÓSTICAS BÁSICAS EN DERMATOLOGÍA ONCOLÓGICA:
Una de las
principales responsabilidades del dermatólogo es el diagnóstico correcto y el
tratamiento eficaz de las neoplasias cutáneas. En ocasiones, el éxito en el
tratamiento puede verse comprometido por una inadecuada selección de la técnica
quirúrgica empleada.
El
objetivo del estudio histológico en la cirugía convencional es el diagnóstico
del tipo de tumor y determinar si éste ha sido o no completamente extirpado. En
este sentido tiene especial interés conocer el método empleado para el estudio
de márgenes, ya que de ello depende en ocasiones el seguimiento a realizar en
el paciente.
A) TÉCNICAS DE BIOPSIA CUTÁNEA[1]:
La biopsia
cutánea es una técnica simple y esencial para establecer o confirmar el diagnóstico
de una neoplasia cutánea que consiste en obtener una muestra de tejido,
adecuada para el examen histológico tratando de originar la menor cicatriz
posible. Permite también, conocer la profundidad y extensión de la lesión, el
subtipo histológico y relacionar estas características con la agresividad biológica
de la lesión.
En
general, las lesiones de tamaño inferior a
PROCEDIMIENTOS DE
1º Limpieza del área quirúrgica " nº de bacterias $
9 Alcohol isopropílico
9 Gluconato de clorhexidina
9 Povidona iodada
2º Administración de un anestésico local
9 LIDOCAÍNA 1 o 2% es el más empleado
3º Obtención de una muestra de tejido
4º Examen histológico
B) MÉTODOS DE BIOPSIA[2]:
1.
BIOPSIA POR REBANADO O AFEITADO:
-
Indicaciones
· lesiones sobreelevadas, pedunculadas o lesiones con
afectación
exclusivamente
epidérmica.
-
Diagnóstico del:
· Carcinoma basocelular, carcinoma epidermoide
· Nunca se puede hacer en: nódulos profundos o
lesiones melánicas
-
Ventajas:
· Rapidez
· Escaso sangrado
-
Inconvenientes " escasa muestra.
2.
BIPOSIA EN SACABOCADOS (Punch):
-
Indicaciones:
lesiones profundas
-
Diagnóstico:
· de pequeñas lesiones melánicas.
· infiltración de estructuras.
-
Ventajas:
determinación óptima de los márgenes.
-
Desventajas:
escasa muestra y resultado cosmético comprometido.
3.
BIOPSIA INCISIONAL:
-
Indicaciones : lesión
cutánea de gran tamaño.
-
Desventajas:
clásicamente se había señalado que la manipulación del tumor durante la
realización de una biopsia incisional incrementaría el riesgo de diseminación
local y regional de células malignas, comprometiendo la supervivencia de
pacientes con melanoma
4.
BIOPSIA ESCISIONAL:
-
Indicaciones:
obtención de una muestra cutánea que incluye la totalidad de la lesión visible
clínicamente:
· Melanoma.
· Tumores malignos.
-
Ventaja: permite
eliminar por completo la lesión sin necesidad de cirugía posterior.
Volver al índice
3.-
CLASIFICACIÓN DE LAS NEOPLASIAS CUTÁNEAS.
3.1.- Carcinomas:
a) Carcinoma
basocelular.
b) Carcinoma
espinocelular.
3.2.- Neoplasias anexiales
cutáneas malignas:
a)
Carcinoma sebáceo.
b)
Carcinoma papilar.
c)
Carcinoma siringoide.
d)
Porocarcinoma.
e)
Carcinoma anexial microquístico.
f)
Carcinoma adenoide quístico.
g)
Carcinoma mucinoso.
3.3.- Melanomas:
3.4.- Sarcoma de Kaposi:
3.5.- Otros angiosarcomas:
a)
Angiosarcoma NO ASOCIADO A LINFEDEMA.
b) Angiosarcoma Cutáneo asociado a
Linfedema (Stewart-Treves).
c)
Angiosarcoma Radioinducido.
d)
Otros:
●
Angiosarcoma epiteloide.
●
Hemangioma endotelioma epiteloide.
●
Hemangioma endotelioma retiforme.
●
Angioendotelioma papilar endovascular (tumor de Dasbska).
Volver al índice
El melanoma ha suscitado una gran atención debido al
gran incremento de su incidencia. En la actualidad sigue sin existir un
tratamiento efectivo para este tumor cuando se ha diseminado. Por tanto la
prevención, la detección temprana y la cirugía continúan siendo los pilares en
el manejo de este tumor.
4.1.- DEFINICIÓN:
El melanoma es un tumor maligno y potencialmente
letal. Se origina a partir de melanocitos que han sufrido un proceso de
malignización por lo que se puede desarrollar en cualquier superficie en la que
haya melanocitos. Por eso aunque el lugar más frecuente es en la piel, el
melanoma también se ha descrito en el epitelio de las mucosas, en la
conjuntiva, en la retina y en las leptomeninges[3].
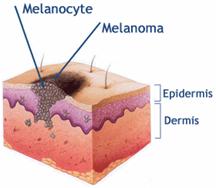
Fig. 2. Estructura de un melanoma.
4.2.- EPIDEMIOLOGÍA[4]:
Desde hace unas décadas, se ha producido un aumento
progresivo de la incidencia del melanoma. Este aumento se ha atribuido
principalmente en las costumbres en relación con el sol, aunque la longevidad
también podría ser un factor adicional.
Las mayores cifras de incidencia se encuentran en
Australia donde la población tiene un fenotipo[5]
cutáneo con predominio de fenotipos bajos y los índices de radiación solar son
muy elevados. Sin embargo la incidencia real es desconocida pues existe un gran
número de melanomas de bajo riesgo que no llegan a conocerse. Además, debido a
las campañas de concienciación y detección precoz se cree que puede haber un
falso aumento, lo que parece estar apoyado porque el aumento de la incidencia
es principalmente debido a un aumento del número de melanomas de pequeño
grosor.
El melanoma representa algo más del 75% de las
muertes producidas por cáncer cutáneo. Aunque la mortalidad por melanoma
también ha experimentado un aumento progresivo, la mayor parte de países
presenta un estancamiento de las tasas de mortalidad excepto para los ancianos.
4.3.- FACTORES DE RIESGO[6]:
En este epígrafe se incluyen tanto las lesiones
precursoras como los marcadores de un mayor riesgo de padecer melanoma:
1-Nevus
melanocítico congénito: En los nevus melanocíticos gigantes, el riesgo de malignización es mayor
antes de 5 años de vida, por lo que se aconseja su exéresis radical precoz. Los
nevus melanocíticos de menor tamaño no se considera justificada su extirpación
con finalidad preventiva.
2-Nevus melanocíticos adquiridos comunes :
Se considera que la presencia de más de 50 nevus adquiridos de más de 2mm
confiere un importante aumento del riesgo relativo de desarrollar un melanoma.
Es así porque la presencia de múltiples nevus esta concidionada por una
predisposición genética y por exposiciones intermitentes al sol.
3-Nevus melanocíticos clínicamente
atípicos: Se entienden como lesiones asimétricas, mal circunscritas,
con varios colores, de mayor tamaño a 5mm y con un componente macular
periférico.
4-Fototipo cutáneo: Las pieles
claras con tendencia a quemarse por el sol (fototipos 1 y 2) presentan un mayor
riesgo de desarrollar un melanoma.
Las
pieles más claras y en especial los pelirrojos, presentan una mayor cantidad de
feomelanina. Este tipo de melanina protege peor del ADN del poder mutagénico de la radiación
ultravioleta.
5-Antecedentes familiares de melanoma:
El 8-12% de los melanomas presentan antecedentes familiares de melanoma. No
existe, sin embargo, una definición precisa del melanoma familiar como existe
en otros cánceres familiares. De cualquier forma, está indicado realizar una
monitorización cutánea a familiares de primer grado de los pacientes con
melanoma.
Se
han identificado diferentes lesiones que parecen contener determinadas
alteraciones que condicionan una susceptibilidad genética al padecer un
melanoma.
6-Antecedentes personales de melanoma:
Los pacientes que tienen un melanoma tienen un mayor riesgo que la población
general al desarrollar otro melanoma.
Este
riesgo hace que un 3-6% de los pacientes tengan un segundo melanoma a lo largo
de su vida. Se han detectado mutaciones en CDKN2A en el 15% de pacientes con
melanomas múltiples, lo que parece demostrar una cierta susceptibilidad genética,
además de la persistencia de otros factores con melanoma.
7-Exposición solar: La forma en
que ha tenido lugar dicha exposición parece determinar la variedad
clínico-patológica a la que se está predispuesto. Así la exposición solar
intermitente, expresada como quemaduras intensas durante la infancia y
adolescencia, o durante los 10 años previos, predispone a padecer un melanoma
de extensión superficial o nodular. Por el contrario, la exposición crónica
acumulada no sólo predispone al léntigo maligno melanoma sino que, incluso,
parece representar una factor de protección para padecer las dos variedades
anteriores.
La
radiación ultravioleta es la responsable del daño celular, especialmente daño
del ADN, lo que parece jugar un papel primordial en la carcinogénesis.
4.4.- FACTORES PRÓNOSTICOS CLÍNICOS,
PATOLÓGICOS Y MOLECULARES[7]:
a) Clínicos:
Sexo: Hay un pronóstico más
favorable en las mujeres que en los hombres. Esta circunstancia parece estar
favorecida por una mayor tendencia a presentar tumores en las piernas.
Localización anatómica: Se
suelen localizar en las extremidades tienen en general un mejor pronóstico. Y
dentro de las extremidades parece existir un gradiente de forma que el
pronóstico es peor cuanto más distal es la localización.
Edad: Hay una menor
supervivencia a partir de los 60 años. Este factor es el tercero en importancia
tras el espesor tumoral y la ulceración en el estudio multivariado cuando se
consideran las variables más fácilmente reproducibles.
b) Patológicos:
Espesor tumoral: El espesor
tumoral medido en milímetros a partir de la capa granulosa representa todavía
el mejor factor pronóstico en el melanoma localizado.
La
relación entre la supervivencia y el grosor tumoral sigue una curva exponencial
sin intervalos naturales con pronóstico similar.
Ulceración tumoral: Es el
segundo factor pronóstico en importancia. Se considera que existe ulceración
cuando la epidermis que recubre el melanoma ha desaparecido y es reemplazada
por un exudado inflamatorio.
Nivel de invasión de Clark:
Se define según la capa de la piel invadida por el melanoma. Es un factor
pronóstico dependiente del espesor tumoral y sólo tiene valor independiente,
superior incluso a la presencia de ulceración, en los melanomas con un Breslow[8] menor
o igual a 1mm.
Patrón de crecimiento: No
parece modificar el pronóstico con la excepción del léntigo maligno melanoma.
En este caso, por causas desconocidas, pacientes con tumores de más de
Invasión perineural: Esta variedad
representa menos del 1% de los casos y tiene la particularidad de invadir
localmente alrededor de los nervios lo que confiere una especial tendencia a la
recurrencia local.
Infiltración linfocitaria: Se
cree que expresa la capacidad de respuesta del organismo frente al melanoma.
Regresión: Las
características están marcadas por una fibrosis en la dermis papilar, numerosos
espacios vasculares dilatados, un número variable de macrófagos y un menor
grado de malignización.
Embolización vascular: El reconocimiento
de la invasión vascular, linfática y sanguínea es, a veces, difícil.
Satelitosis microscópicas: Se
definen como la presencia de nidos de células tumorales de un diámetro mayor de
0’05mm y separados del nódulo tumoral primario por una banda de dermis
reticular o hipodermis normal.
Índice mitósico: Se define
como la cantidad de mitosis por mm2 medida en la zona tumoral con mayor
cantidad de mitosis, calculada como una media de 10 campor de gran aumento.
Tipo celular: El pronóstico
del melanoma en relación con el tipo celular no tiene especial significación,
salvo en los melanomas de células nevoides que parecen tener mejor pronóstico.
c) Moleculares:
Se han estudiado múltiples variables biológicos que
expresan diferentes capacidades de las células tumorales para progresar:
adhesión, crecimiento incontrolado y escape inmunológico. La mayoría de ellas
han demostrado un valor pronóstico importante, en ocasiones superando incluso
al espesor tumoral.
4.5.- CLÍNICA[9]:
El examen clínico es el principal método para
diagnosticar el melanoma. La regla del ABCD es muy importante ya que define las
4 características fundamentales del melanoma: A de asimetría, B de bordes
irregulares, C de heterogeneidad de colores y D para indicar lesiones de un
cierto tamaño, generalmente con un diámetro mayor de 6 milímetros.
Tanto el nevus melanocítico congénito como el nevus
atípico pueden degenerar en un melanoma. El porcentaje de melanomas que se
desarrolla sobre un nevus melanocítico preexistente no puede determinarse
atendiendo sólo a criterios clínicos por eso el examen histológico es capaz de
orientarnos sobre la cuestión de cuántos melanomas se desarrollan sobre nevus
melanocíticos.
4.6.- TIPOS DE MELANOMAS[10]:
Se diferencian 4 tipos de melanomas según los
hallazgos clínicos e histológicos. Existen tres tipos de melanomas con fase de
crecimiento horizontal: el melanoma de
extensión superficial, el lentigo melanoma maligno y el melanoma lentiginoso
acral. El cuarto tipo de melanoma: melanoma
nodular que entra en fase de crecimiento vertical sin pasar previamente por
una fase horizontal.
a) El
melanoma de extensión superficial: supone
el 70% de todos los melanomas. Puede estar localizado en cualquier zona, aunque
sobre todo en piernas en mujeres.
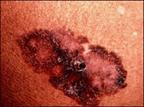 Fig. 3. Melanoma de extensión superficial
Fig. 3. Melanoma de extensión superficial
b) El
melanoma lentiginoso acral: se
localiza en palmas, plantas, la zona periungueal y el lecho de la uña.
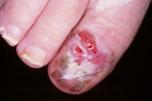 Fig. 4. Melanoma lentiginoso acral.
Fig. 4. Melanoma lentiginoso acral.
c) El
melanoma nodular: aparece en forma
de nódulo redondeado, pigmentado, con un crecimiento rápido, que pasa
directamente a la fase de crecimiento
vertical.
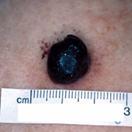 Fig. 5. Melanoma nodular.
Fig. 5. Melanoma nodular.
d) El
lentigo melanoma maligno: es una
lesión macular que crece muy lentamente, de forma que puede mantenerse en esta
localización intraepidérmica durante muchos años antes de romper la membrana
basal e iniciar la fase de invasiva.
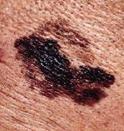 Fig. 6. Lentigo
melanoma maligno.
Fig. 6. Lentigo
melanoma maligno.
4.7.- MÉTODOS DE DIAGNÓSTICO[11]:
Dermatoscopia
Es una técnica diagnóstica no invasiva para el examen
in vivo de las lesiones cutáneas pigmentadas. El método se basa en el reconocimiento
de una serie estructuras y patrones, a partir de los cuales se han desarrollado
las reglas de ABCD o algoritmos que permiten un análisis más objetivo de
cualquier lesión.
Examen histopatológico
Cuando a partir de la clínica, la dermatoscopia, una
lesión plantea la sospecha de un melanoma, debe siempre realizarse una biopsia.
Se aconseja hacer una biopsia excisional mediante un huso. Puede utilizarse un
Punch siempre que se incluya la lesión completa. Las biopsias parciales pueden
estar justificadas en áreas de importancia cosmética como la cara y en lesiones
pigmentadas muy grandes en las que la extirpación completa con un cierre
directo no sería posible.
Los criterios utilizados para diagnosticar un
melanoma pueden dividirse en 2 categorías: arquitecturales y citológicos.
-- Arquitecturalmente, los melanomas
suelen tener más de 5-6mm, son asímétricos, carecen de circunscripción lateral,
los melanocitos pueden observarse sobre la capa basal y el tamaño y la forma de
los nidos no es uniforme.
-- Citológicamente, los núcleos de los
melanocitos son grandes y atípicos. Progresivamente algunos de los melanocitos
ascienden y se disponen en capas más altas de la epidermis.
4.8.- ESTADIAJE:
|
PROPUESTA
DE ESTADIAJE PARA EL MELANOMA CUTÁNEO AMERICAN
JOINT COMMITTEE ON CANCER STAGING SYSTEM 2001. |
|
|
Estadio |
Criterios |
|
0 |
Melanoma
in situ |
|
IA |
Melanoma
localizado, ≤ |
|
IB |
Melanoma
localizado, ≤ |
|
IIA |
Melanoma
localizado, 1,0 - |
|
IIB |
Melanoma
localizado 2,01- |
|
IIC |
Melanoma
localizado, > 4,0 con ulceración |
|
IIIA* |
Micrometástasis
en 1-3 ganglios con melanoma primario no ulcerado |
|
IIIB |
Micrometástasis
en 1-3 ganglios con melanoma primario ulcerado o macrometástasis en 1-3
ganglios con melanoma primario no ulcerado o metástasis en tránsito sin
ganglios metastáticos con cualquier melanoma primario |
|
IIIC |
Macrometástasis
en 1-3 ganglios con melanoma primario ulcerado o > 4 ganglios
metastáticos, o metástasis en tránsito con ganglios metastáticos |
|
IV |
Tres
grupos: M1a: metástasis a distancia cutáneas, subcutáneas o ganglionares.
M1b: metástasis pulmonares. M1c: el resto de las metástasis viscerales o
cualquier metástasis visceral con LDH sérica elevada. |
*
se ha propuesto un estadiaje clínico y otro patológico. No hay subgrupos en el
estadío III en el estadiaje clínico.
Fig. 7. Estadíos del melanoma.
4.9.- PRONÓSTICO:
|
SUPERVIVENCIA
DE LOS PACIENTES CON MELANOMA TENIENDO EN CUENTA LOS DATOS HISTOPATOLÓGICOS
PARA EL ESTADIAJE. |
|
|
Estadio patológico |
Supervivencia a los cinco años |
|
IA |
95
% |
|
IB |
90
% |
|
IIA |
78
% |
|
IIB |
65
% |
|
IIC |
45
% |
|
IIIA |
66
% |
|
IIIB |
52
% |
|
IIIC |
26
% |
|
IV |
9
– 18 % |
Fig. 8. Porcentaje de supervivencia de los diferentes
estadíos del melanoma.
4.10.- TRATAMIENTO[13]:
Cirugía
Debido
a que las células del melanoma pueden migrar individualmente lejos del tumor
primario, éste puede extenderse en profundidad o lateralmente más allá de lo
que se percibe clínicamente. Por ello, las recomendaciones para la extirpación
incluyen siempre la inclusión de un margen de piel normal alrededor del tumor
para asegurar su extirpación completa.
Las
recomendaciones más recientes de
|
RECOMENDACIONES PARA EL TRATAMIENTO
QUIRÚRGICO DEL MELANOMA |
|
|
Espesor tumoral |
Márgenes de extirpación |
|
In situ |
0’5 |
|
< |
1 |
|
> |
2 |
Fig. 9. Márgenes de extirpación en el tratamiento quirúrgico
del melanoma según el espesor tumoral.
Debe
realizarse una extirpación en profundidad hasta la fascia, sin necesidad de
incluir esta.
Respecto
a la disección ganglionar debemos diferenciar tres contextos. La linfadenectomía[14]
terapéutica se refiere al vaciamiento ganglionar de una cuenca
linfática cuando se detecta clínicamente por palpación que algún ganglio está
afecto. La linfadenectomía profiláctica o electiva supone la extirpación
de todos los ganglios linfáticos de la cadena linfática de drenaje del
melanoma, aunque estos ganglios no se palpen. En la última década, la linfadenectomía
selectiva ha ganado una gran aceptación como forma de tratamiento para
aquellos melanomas de espesor intermedio. Ésta se basa en el concepto del
ganglio centinela. Este ganglio es el primero en recibir el drenaje linfático
de un tumor, es decir, el primero colocado en la ruta de drenaje linfático del
tumor.
Tratamiento adyuvante
Actualmente,
el interferón alfa es el único tratamiento adyuvante que ha demostrado ser
efectivo en términos de supervivencia global y supervivencia libre de
enfermedad. En los pacientes de alto riesgo con metástasis ganglionares, las
dosis altas de interferón alfa han demostrado una mejora tanto en la
supervivencia global como en la supervivencia libre de enfermedad. El
interferón alfa se considera también apropiado para otros pacientes con
melanoma de alto riesgo, como aquellos con metástasis en tránsito o los que no
tienen metástasis ganglionares pero su melanoma tenía un espesor superior a
cuatro milímetros, sin embargo, es muy tóxico.
Tratamiento sistémico
Cuando
el melanoma sea diseminado sistémicamente, es uno de los cánceres con mayor
mortalidad y no existe un tratamiento satisfactorio. No hay un tratamiento
estándar para el melanoma metastático, y cada caso debe evaluarse de forma
individual. La cirugía debe plantearse en aquellos pacientes con enfermedad
limitada sin afectación visceral o limitada a alguna metástasis pulmonar,
siempre y cuando se haya documentado que ha transcurrido un período de tiempo
razonable sin progresión de la enfermedad.
La
radioterapia es una opción como tratamiento paliativo en los casos de lesiones
cutáneas dolorosas o en grandes tumores que causen sangrado, compresión
vascular o neurológica. En pacientes de edad avanzada con enfermedades
sistémicas invalidantes en los que el melanoma se ha diseminado o en aquellos
que no han respondido a otros tratamientos debe considerarse la posibilidad de
limitarse a cuidados paliativos.
De
todas formas, para pacientes con enfermedad diseminada, los principales
tratamientos son: la quimioterapia, los modificadores de repuesta biológica
(MRB) y combinación de quimioterapia y MRB que recibe el nombre de
bioquimioterapia. La dacarbazina[15]
(DTIC) sigue siendo el tratamiento estándar de primera línea en el melanoma
metastásico.
Volver al índice
“Neoplasia
multifocal y primariamente cutánea”
Recibió
el nombre a partir de un dermatólogo húngaro llamado Moritz Kaposi. Al
principio se considero al SK como una neoplasia progresiva y potencialmente
fatal; pero ya se han descrito cuatro variedades con pronóstico y clínica
diferentes.
En
los últimos años se han producido importantes avances sobre este tumor, principalmente
con relación a la implicación del virus herpes tipo 8 en su etiopatogenia.
5.1. VARIEDADES CLINICAS DEL SK[16]:
l Variedad CLÁSICA:
Frecuente
en varones de edad avanzada procedentes de países ribereños del Mediterráneo o
del Este de Europa. Las lesiones más incipientes son máculas que luego
evolucionan hacia la formación de placas y nódulos, de color azul o rojo
oscuro. Dichas lesiones se localizan en pies, tobillos, manos... que
posteriormente progresan en sentido proximal. Esto acaba con la instauración de
linfedema en el miembro afecto.
lVariedad ENDÉMICA:
Se
solapaba con el área de máxima incidencia de linfoma de Burkitt. En la década
de los 80, coincidió con la epidemia del VIH se produjo un súbito aumento de la
incidencia de SK en determinados países. En la actualidad es el tumor más
frecuente en algunos países de África central.
l Variedad en relación con
pacientes TRANSPLANTADOS:
Variedad
relacionada con pacientes inmunodeprimidos, que están sometidos a tratamientos
con ciclosporinas, azatriopina, corticosteroides... para prevenir el rechazo de
un transplante. Este grupo de SK tiene relación con hombres de ascendencia
mediterránea, semítica o africana. Suele ser agresivo, afectando a los ganglios
linfáticos, las mucosas y los órganos viscerales y aparece tras un intervalo de
l Variedad EPIDÉMICA
asociada al VIH (homosexuales):
Principalmente
afecta a varones homosexuales que padecen enfermedades oportunistas severas y
una importante depresión de la inmunidad mediada por las células. Afecta a
piel, ganglios linfáticos, vísceras y mucosas.
El
riesgo de SK en pacientes con SIDA es muy elevado al compararlo con la
población general; pero actualmente su incidencia ha disminuido
progresivamente.
5.2. HISTOLOGÍA[17]:
-
Independientemente a la variedad clínica que se trate, el diagnóstico
histológico se separa en las dos fases principales del desarrollo del SK:
I)
Fase INICIAL
Hay
una proliferación de pequeños vasos dilatados e interconectados en la dermis
superior que rodean a los anejos y a los vasos normalmente presentes en esta
zona. Conjuntamente se observa un infiltrado inflamatorio constituido por
linfocitos y células plasmáticas.
II)
Fase en estadio de PLACA
Fácilmente
reconocible; el componente vascular es más difuso, afectando a toda la dermis
con disección de las fibras de colágeno. Los vasos desarrollan estructuras
diferentes, algunos están interconectados entre sí y tienen una apariencia
similar a los canales linfáticos, mientras que otros contienen hematíes y se
parecen a los vasos sanguíneos.
Se
observan nódulos bien definidos en los que se encuentran: fascículos de células
fusiformes y estructuras vasculares.
5.3. ETIOPATOGENIA[18]: Virus Herpes humano 8 (VHH 8)
-
En 1994 Chang y cols. Identificaron fragmentos de ADN de un virus herpes
previamente no conocido; este virus se ha demostrado que es el VHH 8,
perteneciente a la subfamilia de los virus herpes gamma.
-
Pero también es sabido que se necesitan otras condiciones para la aparición de
los tumores. Por lo tanto, el SK se desarrolla por la infección de este virus y
por la conjunción en mayor o menor grado de determinados factores (según la
variedad a la que nos refiramos): inmunodepresión, papel coadyuvante del virus VIH
y predisposición genética.
5.4. DIAGNÓSTICO
Y DIAGNÓSTICO DIFERENCIAL[19]:
-
Es fundamental realizar
una biopsia para confirmarlo, una exploración general del paciente, radiografía
del tórax y una analítica que incluya hemograma.
-
El diagnóstico
diferencial clínico del SK debe establecerse en las siguientes entidades:
granuloma piogénico, vasculitis, angiomitosis bacilar, angiosarcoma, linfesema,
celulitis y queloide.
-
Se han desarrollado
varias clasificaciones para estudiar a los pacientes, 2 grupos a los que
denomina de mal o buen pronóstico con arreglo a 3 factores:
· Extensión del tumor.
· Sistema inmunitario.
· Estado general
(si hay enfermedad sistémica o no).
5.5. TRATAMIENTO[20]:
I)
SK Clásico:
-
Para pacientes con
lesiones únicas, el tratamiento adecuado es la extirpación quirúrgica.
-
La radioterapia es el
tratamiento de elección para aquellos pacientes con múltiples lesiones, siempre
que estén limitadas a un área anatómica.
-
Los pacientes con
enfermedad diseminada o con afectación ganglionar, necesitan un tratamiento
combinado con cirugía, radioterapia y quimioterapia; teniendo buenos resultados.
II)
SK Endémico:
Se usa la quimioterapia con uno o varios fármacos
(doxorrubicina, bleomicina), pero tienen un mal pronóstico y una supervivencia
de sólo unos años.
III)
SK asociado a
pacientes transplantados:
El tratamiento inmediato para pacientes que están
tomando fármacos inmunodepresores, es la retirada inmediata o disminución de
dicho tratamiento. Con lo cual, hay problemas de pérdida del transplante renal
en un 50 % de los casos.
IV) SK Epidémico:
Las actuales terapias antirretrovirales mejoran la
inmunodepresión de los pacientes con SIDA, disminuyendo la carga viral del VIH
y aumentando las cifras de linfocitos CD4. Con esta terapia se consigue una
estabilización o reducción de las lesiones de SK.
Si no responde a los retrovirales, se valora el
tratamiento con quimioterapia.
5.6. PRONÓSTICO[21]:
-
SK clásico:
pronóstico bueno, ya que la enfermedad es lentamente progresiva y las personas
afectadas son de elevada edad, con lo que no suelen fallecer por causas
relacionadas con el SK.
-
SK endémico:
peor pronóstico. Supervivencia inferior a los 3 años.
-
SK asociado a
pacientes transplantados: pronóstico peor que el SK clásico.
-
SK asociado a VIH:
el pronóstico ha mejorado al introducir las efectivas terapias antirretrovirales
actuales, especialmente con la terapia HAART.
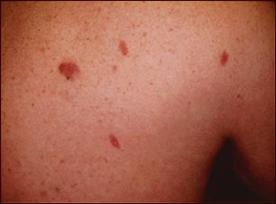
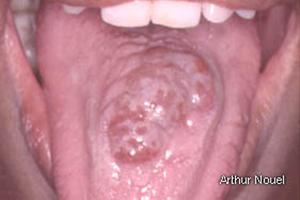
Fig. 10.
Lesiones de Sarcoma de Kaposi en espalda.
Fig. 11. Lesiones de Sarcoma de Kaposi en lengua.
Volver al índice